Fosforescência é a luminescência que ocorre quando energia é fornecido por radiação eletromagnética, geralmente luz ultravioleta. A fonte de energia chuta um elétron de um átomo de um estado de energia mais baixo para um estado de energia mais alto "excitado"; então o elétron libera a energia na forma de luz visível (luminescência) quando volta a um estado de energia mais baixo.
Principais tópicos: fosforescência
- A fosforescência é um tipo de fotoluminescência.
- Na fosforescência, a luz é absorvida por um material, elevando os níveis de energia dos elétrons para um estado excitado. No entanto, a energia da luz não combina com a energia dos estados excitados permitidos, de modo que as fotos absorvidas ficam presas em um estado triplo. As transições para um estado de energia mais baixo e mais estável levam tempo, mas quando ocorrem, a luz é liberada. Como essa liberação ocorre lentamente, um material fosforescente parece brilhar no escuro.
- Exemplos de materiais fosforescentes incluem estrelas que brilham no escuro, alguns sinais de segurança e tinta brilhante. Ao contrário dos produtos fosforescentes, os pigmentos fluorescentes param de brilhar depois que a fonte de luz é removida.
- Embora nomeado para o brilho verde do elemento fósforo, o fósforo realmente brilha por causa da oxidação. Não é fosforescente!
Explicação Simples
A fosforescência libera a energia armazenada lentamente ao longo do tempo. Basicamente, o material fosforescente é "carregado", expondo-o à luz. Então a energia é armazenada por um período de tempo e liberada lentamente. Quando a energia é liberada imediatamente após a absorção da energia incidente, o processo é chamado fluorescência.
Explicação da Mecânica Quântica
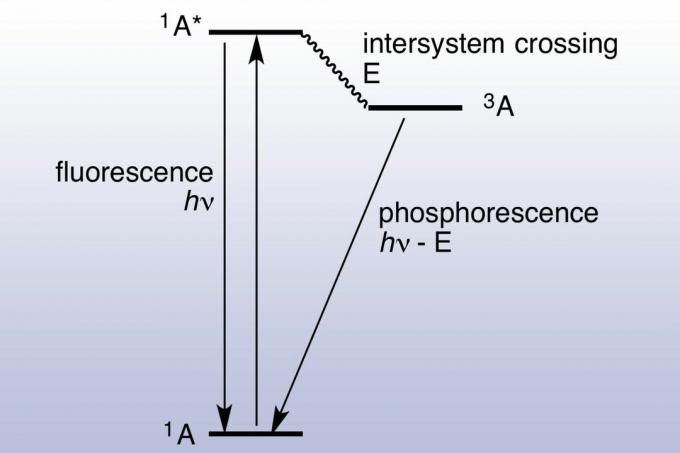
Na fluorescência, uma superfície absorve e reemite um fóton quase instantaneamente (cerca de 10 nanossegundos). A fotoluminescência é rápida porque a energia dos fótons absorvidos corresponde aos estados de energia e permite transições do material. A fosforescência dura muito mais (milissegundos até dias) porque o elétron absorvido passa para um estado excitado com maior multiplicidade de rotação. Os elétrons excitados ficam presos em um estado tripleto e só podem usar transições "proibidas" para cair para um estado singleto de energia mais baixa. A mecânica quântica permite a transição proibida, mas não é cineticamente favorável, portanto leva mais tempo para ocorrer. Se luz suficiente é absorvida, a luz armazenada e liberada se torna suficientemente significativa para que o material pareça "brilhar no escuro ". Por esse motivo, materiais fosforescentes, como materiais fluorescentes, aparecem muito brilhantes sob uma luz negra (ultravioleta). Um diagrama de Jablonski é comumente usado para exibir a diferença entre fluorescência e fosforescência.
História
O estudo de materiais fosforescentes remonta a pelo menos 1602 quando o italiano Vincenzo Casciarolo descreveu um "lapis solaris" (pedra do sol) ou "lapis lunaris" (pedra da lua). A descoberta foi descrita no livro de 1612 do professor de filosofia Giulio Cesare la Galla De Fenômeno em Orbe Lunae. La Galla relata que a pedra de Casciarolo emitiu luz depois de ter sido calcificada por aquecimento. Ele recebeu luz do Sol e depois (como a Lua) emitiu luz na escuridão. A pedra era barita impura, embora outros minerais também exibissem fosforescência. Eles incluem alguns diamantes (conhecido pelo rei indiano Bhoja em 1010-1055, redescoberto por Albertus Magnus e novamente redescoberto por Robert Boyle) e topázio branco. Os chineses, em particular, valorizavam um tipo de fluorita chamado clorofano que exibia luminescência do calor do corpo, exposição à luz ou sendo esfregado. O interesse na natureza da fosforescência e outros tipos de luminescência acabou levando à descoberta da radioatividade em 1896.
Materiais
Além de alguns minerais naturais, a fosforescência é produzida por compostos químicos. Provavelmente o mais conhecido deles é o sulfeto de zinco, que tem sido usado em produtos desde a década de 1930. O sulfeto de zinco geralmente emite uma fosforescência verde, embora possam ser adicionados fósforos para alterar a cor da luz. Os fósforos absorvem a luz emitida pela fosforescência e depois a liberam como outra cor.
Mais recentemente, o aluminato de estrôncio é usado para a fosforescência. Este composto brilha dez vezes mais que o sulfeto de zinco e também armazena sua energia por muito mais tempo.
Exemplos de fosforescência
Exemplos comuns de fosforescência incluem estrelas colocadas nas paredes dos quartos, que brilham por horas depois que as luzes se apagam e tinta usada para fazer murais brilhantes. Embora o elemento fósforo brilha em verde, a luz é liberada da oxidação (quimioluminescência) e é não um exemplo de fosforescência.
Fontes
- Franz, Karl A.; Kehr, Wolfgang G.; Siggel, Alfred; Wieczoreck, Jürgen; Adam, Waldemar (2002). "Materiais luminescentes" em Enciclopédia de Química Industrial de Ullmann. Wiley-VCH. Weinheim. doi: 10.1002 / 14356007.a15_519
- Roda, Aldo (2010). Quimiluminescência e Bioluminescência: Passado, Presente e Futuro. Sociedade Real de Química.
- Zitoun, D.; Bernaud, L.; Manteghetti, A. (2009). Síntese por microondas de um fósforo de longa duração. J. Chem. Educ. 86. 72-75. doi: 10.1021 / ed086p72